- 水的哪些特性使其對地球上的生命至關重要?
- 地球水資源的現狀如何?
- 當今世界水資源的質量對人類有甚麼主要影響?
水在我們的星球上是如此普遍,以至於它的非凡特性經常被忽視。它佔人體質量近70%和植物體質量的95%。水有助於使地球適合生物體居住,並在生理過程中發揮重要作用。水的這些令人難以置信的特徵都始於分子。
水的結構
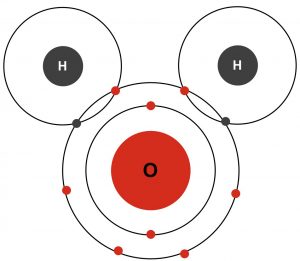
水分子 (H2O)包含兩個氫原子與一個氧原子,每個氫原子與一個氧原子共享一對電子(見圖 1)。當原子以這種方式共享電子時,就會產生共價鍵。這些化學鍵對生物體來說是必不可少的。
在水分子中,氧原子和氫原子共享電子是不平等的。總是帶有負電荷的電子更容易被氧原子吸引。因為共享電子花更多時間環繞氧原子的原子核上,而花更少時間在氫原子的原子核上,水分子變得極化,具有明顯的負極(氧)端和正極(氫)端。這種特性被稱為分子極性。
由於正負電荷相互吸引,當極性水分子相互靠近時,它們會排成一條直線——一個分子的正電氫端被吸引到另一分子的負氧端。這種引力稱為氫鍵(見圖 2)。水分子通過弱氫鍵鬆散地結合在一起,這使得水具有液態性質。如果氫鍵更強,水就會是一種剛性物質,而不是流體物質。
仔細看看
這篇在賓夕法尼亞大學 E.R. 約翰遜研究基金會(E.R. Johnson Research Foundation)發表的論文對水的結構和特性進行了更深入的描述論文對水的結構和特性進行了更深入的描述。
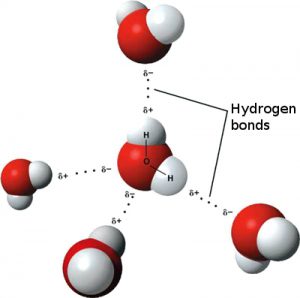
一滴水含有數萬億個由弱氫鍵結合在一起的水分子。水分子結合的傾向稱為內聚力。水分子使用弱氫鍵凝聚使水具有流體的稠度。
水的極性也使它具有黏性,這意味著它會被帶有正負電荷的其他類型分子所吸引。想想樹木如何在沒有泵的情況下將水從土壤中輸送到高高的樹枝上。水分子進入根部,黏附在構成植物傳導組織木質部細胞壁的分子上,木質部細胞形狀像細小的吸管。水在木質部的另一端─葉子─蒸發到空氣中,對整個水柱產生向上的凝聚拉力,取代蒸發了的水份。
前瞻

內聚力和附著力是水最顯著的特性之一。它們足夠強大,可以抵抗重力,讓水流動數百英尺高的樹頂。 這種運動稱為毛細管作用,是植物通過體內輸送液體的關鍵方式。
水溶性
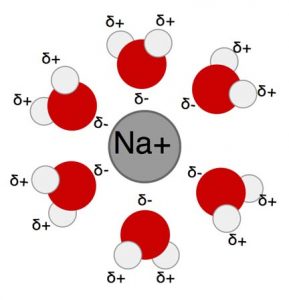
溶劑是一種能夠溶解其他物質的物質。水是一種通用溶劑,因為它能夠溶解大多數其他極性物質。在煮意大利麵或米飯之前,你有沒有在水中加入食鹽?如果有,你可能會注意到鹽最終似乎「消失」了。
前瞻

水的三種物理狀態
水是地球上唯一以三種物理狀態自然存在的物質:固體、液體和氣體(見圖4)。根據溫度和大氣壓力,水可以從一種狀態變為另一種狀態,這一過程稱為物理相變。正因為如此,世界上的一些地理區域會經歷潮濕、下雨、下雪,甚至三者的組合。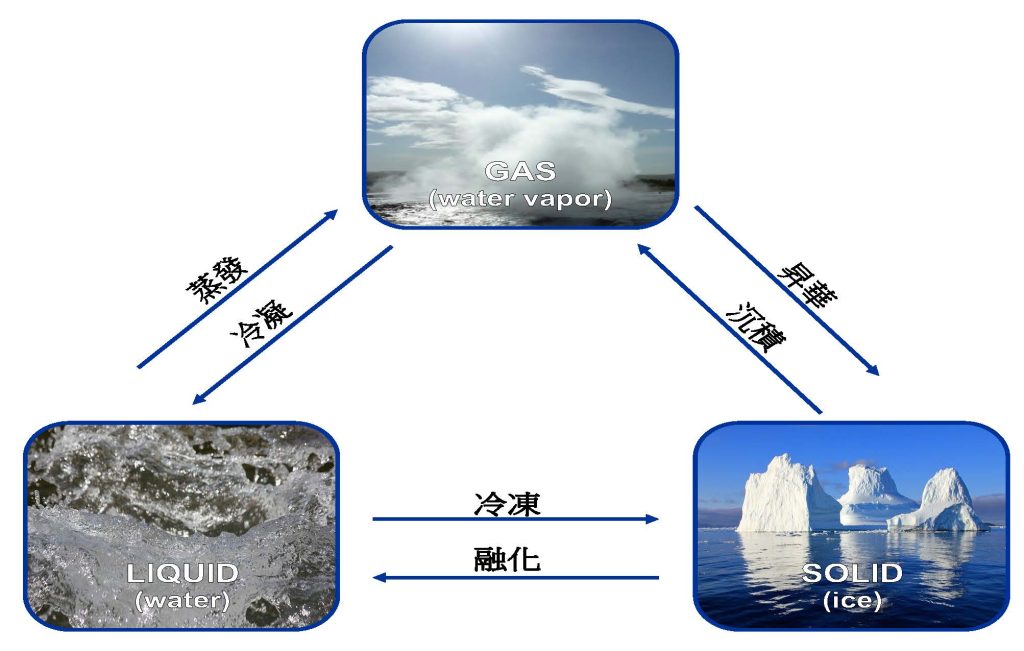
仔細看看

水蒸氣中的水分子幾乎沒有氫鍵,它們之間的空間更大,這使得水蒸氣比水或冰更輕且密度更小。雖然液態水中的H2O分子比在固態冰中更緊密,但液態水中的氫鍵比堅硬的冰晶格中的氫鍵少。因此,水是流動而冰是固體。這視頻演示了水分子的三種形態。
氫鍵再次成為關鍵。分子間的鍵數決定了水是固體、液體還是氣體。在固態下,水分子擁有最多的氫鍵(每個分子4個),使水具有冰的剛性特徵。在液態時,水的氫鍵較少,這解釋了其結構更鬆散和流體性質。
當水從固體變為液體再變成氣體,氫鍵就會斷裂,使水分子更自由地運動。水的這種循環狀態是水文循環的基礎,這對地球上的生命至關重要,它淨化了水並將其分佈到陸地上。這個重要的循環將在下面的「水文循環」部分討論。
水的密度
水是地球上為數不多的固體密度小於液體的物質之一。就像冰一樣,水分子會形成四個氫鍵,將它們鎖定在堅硬的晶體結構中。在這種狀態下,水分子之間的距離實際上比它們處於液態時分開得更遠。這就是為什麼水在結冰時會膨脹,密度比周圍液態水小。由於固體水的密度較小,冬天冰漂浮在湖面上,使湖面下的水不結冰,這對水生生物至關重要。如果固體水比液體水密度大,那麼湖泊和池塘在冬天就會全部結冰,不再提供能存活的棲息地。
事實上,極地和溫帶地區的魚類和其他物種已經進化到可以生活在室外溫度低於水的冰點(32ºF,0ºC)的湖泊。這些水生生物對全年的溫度變化具有相對大的耐受性。然而,物種適應的耐受範圍正受到全球氣候變化引起的溫度變化威脅。關於全球氣候變化對水的影響,我們將在下文和第6章作詳細介紹。